In 1984 verklaarde Marget Heckler1 als minister van het United States Department of Health and Human Services2 (HHS) dat er binnen de twee jaar een HIV-vaccin zou zijn, met de gevleugelde woorden:
Yet another terrible disease is about to yield to patience, persistence and outright genius.
In 1997 richtte Bill Clinton onder het National Institutes of Health3 (NIH) een nieuw onderzoekscentrum op met als doel om een HIV-vaccin te ontwikkelen. Tijdens zijn openingsrede zei hij:
It is no longer a question of whether we can develop an AIDS vaccine, it is simply a question of when.
In 2005 startte Merck klinische tests met een HIV-vaccin. Deze tests werden echter na twee jaar alweer stopgezet omdat ze hadden uitgewezen dat het vaccin het risico op een HIV-infectie eigenlijk alleen maar deed toenemen bij bepaalde recipiënten.
Ondanks die enorme investeringen en de vele klinische tests die nog lopen, zijn we op vandaag nog altijd ver verwijderd van een HIV-vaccin en moeten 35 miljoen mensen nog steeds leren leven met de ziekte. Wetenschappers hebben grote vooruitgang geboekt bij het ontwikkelen van efficiënte antiretrovirale therapieën4 — drugscocktails die de symptomen van geïnfecteerde patiënten stabiliseren. Deze therapieën genezen echter de AIDS-patiënten niet en kunnen ook de verdere verspreiding van HIV niet voorkomen, waardoor de belofte van een vaccin dat de AIDS-epidemie kan indammen vooralsnog niet is ingelost.
Omdat HIV zo snel muteert, kunnen verschillende HIV-isolaten uiteenlopende fenotypen hebben die elk met een aangepaste cocktail van medicijnen moeten behandeld worden. HIV-virussen kunnen bijvoorbeeld onderverdeeld worden in syncytiuminducerende (SI) isolaten die snel repliceren en niet-syncytiuminducerende (NSI) isolaten die traag repliceren. Tijdens de infectie worden virale eiwitten zoals gp1205 — die door HIV gebruikt worden om de cel binnen te dringen — naar het celoppervlak getransporteerd, waar ze het celmembraan van de gastheer kunnen laten samensmelten met dat van naburige cellen. Dit zorgt ervoor dat de celmembranen van tientallen menselijke cellen samensmelten tot één gigantisch, niet-functionerend syncytium of een abnormale multinucleaire cel (zie figuur). Dit mechanisme maakt het ook mogelijk dat een SI-virus meerdere menselijke cellen kan doden door er slechts één enkele te infecteren.
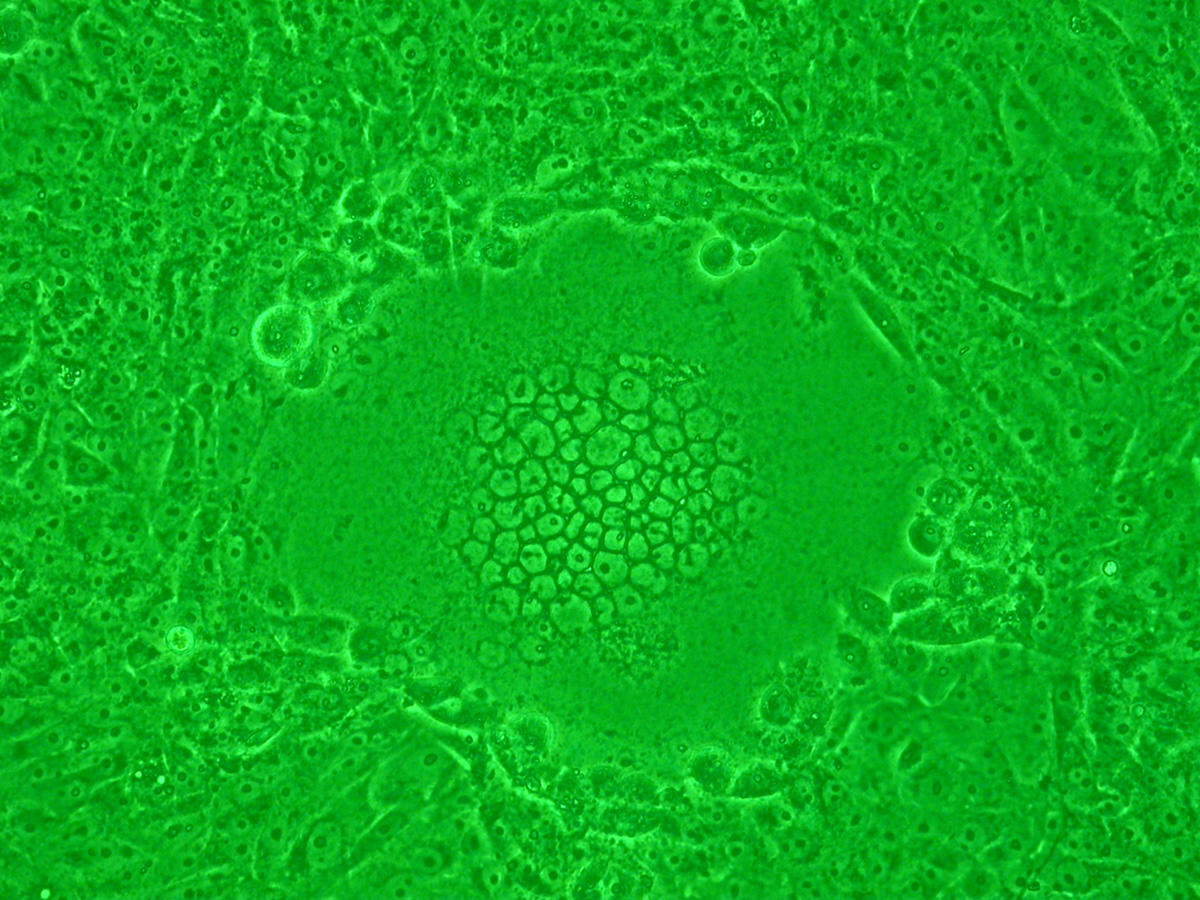
Omdat gp120 belangrijk is bij het classificeren van een HIV virus als SI of NSI, zijn biologen geïnteresseerd in het bepalen van de aminozuren in gp120 die voor deze classificatie kunnen gebruikt worden. In 1992 onderzochten Foucier et al. een meervoudige alignering van het gebied rond de V3-lus in gp120 en stelden op basis daarvan de 11/25 regel op, die stelt dat een HIV-stam vermoedelijk een SI-fenotype heeft als minstens één van de twee aminozuren op posities 11 of 25 van de V3-lus gelijk zijn aan arginine (R) of lysine (K).
CMRPGNNTRKSIHMGPGKAFYATGDIIGDIRQAHC CMRPGNNTRKSIHMGPGRAFYATGDIIGDTRQAHC CMRPGNNTRKSIHIGPGRAFYATGDIIGDIRQAHC CMRPGNNTRKSIHIGPGRAFYTTGDIIGDIRQAHC CTRPNNNTRKGISIGPGRAFIAARKIIGDIRQAHC CTRPNNYTRKGISIGPGRAFIAARKIIGDIRQAHC CTRPNNNTRKRIRMGPGRAFIAARKIIGDIRQAHC CVRPNNYTRKRIGIGPGRTVFATKQIIGNIRQAHC CTRPSNNTRKSIPVGPGKALYATGAIIGNIRQAHC CTRPNNHTRKSINIGPGRAFYATGEIIGDIRQAHC CTRPNNNTRKSINIGPGRAFYATGEIIGDIRQAHC CTRPNNNTRKSIHIGPGRAFYTTGEIIGDIRQAHC CTRPNNNTRKSINIGPGRAFYTTGEIIGNIRQAHC CIRPNNNTRGSIHIGPGRAFYATGDIIGEIRKAHC CIRPNN-TRRSIHIGPGRAFYATGDIIGEIRKAHC CTRPGSTTRRHIHIGPGRAFYATGNILGSIRKAHC CTRPGSTTRRHIHIGPGRAFYATGNI-GSIRKAHC CTGPGSTTRRHIHIGPGRAFYATGNIHG-IRKGHC CMRPGNNTRRRIHIGPGRAFYATGNI-GNIRKQHC CMRPGTTTRRRIHIGPGRAFYATGNI-GNIRKAHC
Opgave
Een eiwit wordt voorgesteld als een opeenvolging van hoofdletters, waarbij de hoofdletters corresponderen met de individuele aminozuren van het eiwit.
Een afwijking van een eiwit wordt beschreven door een string die bestaat uit de cijfers van een getal $$p \in \mathbb{N}_0$$ gevolgd door één of meer hoofdletters. Het getal $$p$$ geeft de positie van de afwijking in het eiwit aan, waarbij de posities van de aminozuren van links naar rechts genummerd worden vanaf 1. Het eiwit vertoont de afwijking als het aminozuur op de aangegeven positie $$p$$ correspondeert met één van de hoofdletters uit de beschrijving van de afwijking. Zo vertoont een eiwit een afwijking 11KR als het elfde aminozuur van het eiwit lysine (K) of arginine (R) is.
Invoer
De eerste drie regels van de invoer bevatten de volgende gegevens:
-
de opeenvolgende aminozuren van een eiwit $$e$$
-
een getal $$m \in \mathbb{N}_0$$
-
een getal $$n \in \mathbb{N}_0$$ ($$n \geq m$$)
Daarna volgen nog $$n$$ regels die elk een afwijking van het eiwit beschrijven. Alle posities $$p$$ van deze afwijkingen zijn verschillend.
Uitvoer
Schrijf een diagnose uit op basis van de afwijkingen die het gegeven eiwit $$e$$ vertoont. De diagnose is positief als het eiwit $$e$$ minstens $$m$$ afwijkingen vertoont, anders is de diagnose negatief. Na de diagnose volgt nog een spatie en tussen ronde haakjes het aantal afwijkingen dat het eiwit $$e$$ vertoont.
Voorbeeld
Invoer:
CMRPGNNTRKSTHMGPGKAFYAICDTIGDIRGAHC
1
2
11KR
25KRUitvoer:
negatief (0)Voorbeeld
Invoer:
CVRPNNYTRKRIGIGPGRTVFATKQIIGNTRQAHC
1
2
11KR
25KRUitvoer:
positief (1)Voorbeeld
Invoer:
CTRPNNNTRKRTSIIGPGRAFTAARKTIGDIRQAHC
1
2
11KR
25KRUitvoer:
positief (2)